“L’editing genomico sarà la medicina del futuro e, al momento, ci sono tutte le premesse per far sì che tecniche di questo tipo possano avere l’effetto sperato”: queste sono le parole che il Professor Rodolfo Ippoliti dell’Università Degli Studi dell’Aquila ha pronunciato a conclusione del suo approfondito discorso relativo all’editing genomico dalla biologia alla medicina.
Quando parliamo di editing genomico, parliamo di quello che molti esperti denominano come la “punta di diamante” delle applicazioni tecnologiche relative al mondo della medicina. Non si tratta però di un argomento facile, facciamo infatti risalire gli studi che ci hanno portato verso questa nuova branca della scienza a molto lontano. È con Mendel, due secoli fa, che la genetica ha iniziato il suo corso; infatti, dagli esperimenti con le piante di piselli del biologo tedesco, siamo arrivati alla scoperta della struttura del DNA nel 1953 da parte di James Watson e Francis Crick e agli studi relativi al DNA ricombinante del 1972. In questo lungo percorso molti studiosi e scienziati hanno dato il loro contributo per arrivare fino al giorno d’oggi, in cui possiamo dire di aver raggiunto un punto di svolta: è nata la cosiddetta ingegneria genetica. Essa ci ha dato e ci continua tutt’oggi a dare grandi soddisfazioni, ma di cosa si tratta? Ed in che modo essa può essere utile in campo medico? Sicuramente le risposte a queste domande sono esplicative riguardo l’argomento trattato, ma per comprenderle al meglio dobbiamo avere conoscenze base riguardo la struttura del nucleo cellulare e, più in particolare, riguardo il DNA.
Il DNA è un polimero formato da due catene antiparallele che insieme ai nucleotidi formano una struttura a doppia elica. Con l’avvitarsi su sé stessi, i due filamenti lasciano scoperti dei solchi, precisamente due: il grande ed il piccolo solco. Tenete bene a mente queste due strutture perché saranno fondamentali per comprendere la maggior parte dei meccanismi di editing che verranno trattati successivamente.

L’editing genomico è una tecnologia altamente innovativa che funziona come un “correttore di bozze” del DNA: interviene in maniera precisa per trovare ed eliminare gli errori all’interno del genoma, come ad esempio per i tumori. Sostanzialmente esso permette di correggere un gene difettoso direttamente là dove si trova senza doverne fornire una copia sana dall’esterno. Per raggiungere particolari punti, questi sistemi sono guidati o da proteine oppure da frammenti di RNA.
Per quanto riguarda i sistemi a guida proteica, già dai primi anni 2000, le tecniche più popolari sono le “nucleasi a dita di zinco”, anche chiamate “zinc fingers” e i TALEN, capaci di agire sui genomi con grande precisione, ma che richiedono anche lunghi periodi di progettazione.
La tecnologia delle Zinc Finger Nucleases permette di operare in modo preciso nel genoma, un sogno fino a poco tempo fa.
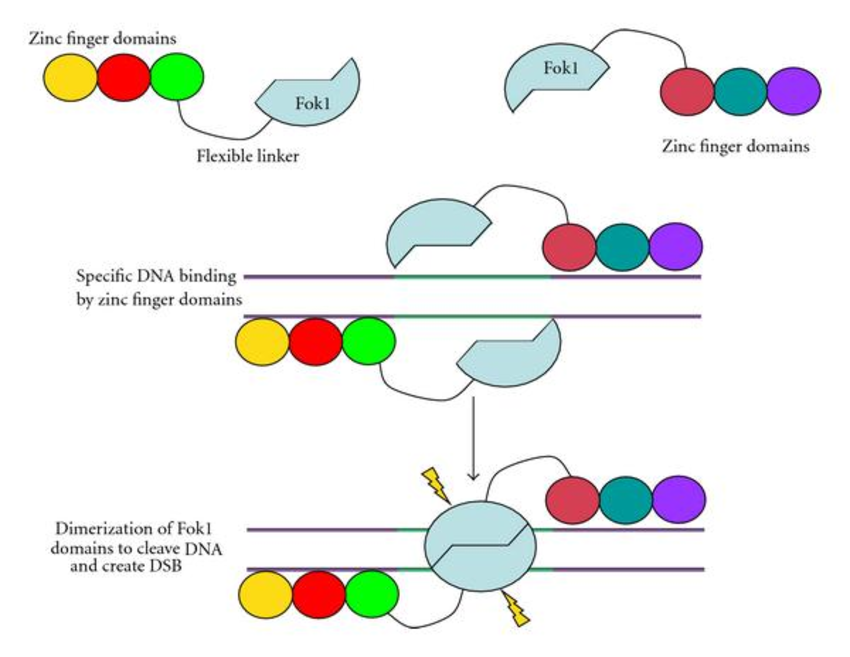
Le ZFN sono proteine costruite affinché possedessero due tipi di attività: riconoscimento di una specifica sequenza di DNA (la sequenza che vogliamo modificare) e taglio del DNA una volta avvenuto il legame.
Pezzettini molto corti di sequenza possono essere letti da proteine che, scorrendo su l’elica del DNA come un dito su una superficie con dei rilievi, riconoscono “cosa c’è scritto”, legandosi saldamente ad alcune sequenze piuttosto che ad altre.
La domanda sorge spontanea: come fanno tali proteine a riconoscere i nucleotidi? La caratteristica che distingue le unità specifiche del DNA è insita nella sequenza in cui si trovano le basi azotate (adenina, timina, guanina e citosina). Le porzioni che si affacciano sul solco maggiore sono differenti rispetto a quelle che si affacciano sul solco minore e sono le uniche che possono essere riconosciute dal gruppo proteico utilizzato per questa operazione.
Tra i motivi proteici in grado di leggere il DNA, un tipo ha proprio la forma di “dito” che scorre lungo l’elica, e si chiama per l’appunto zinc finger, ossia “dito di zinco” (le “dita” sono mantenute in struttura da ioni zinco).
A questo punto è possibile costruire delle proteine artificiali in laboratorio, specifiche per ciascuna sequenza; ma non è finita qua!!
Unendo queste ad una proteina che di mestiere taglia il DNA, chiamata TALEN, che si comporta come una sorta di forbice molecolare, si apre una spaccatura.
Ma come si arriva a modificare il DNA? Per ora abbiamo solo spaccato tutto… dove vogliamo arrivare? Il DNA si comporta come una ferita che si rimargina, le ZFN infatti, servono a sfruttare i naturali meccanismi di riparazione della doppia elica, ed utilizzarli per riparare il danno andando a sostituire alla sequenza mutata quella artificiale, permettendo di risolvere il problema.
Non dimentichiamoci però dell’altra tipologia di sistemi genetici, quelli guidati da frammenti di RNA… e non immaginerete mai come è nata questa intuizione!
La scoperta delle potenzialità dell’RNA è stata il frutto di un lavoro di ricerca botanica che aveva lo scopo di rendere il colore dei petali di petunia più sgargiante. Si voleva infatti aggiungere copie extra del gene colore, ma si è notato che il fiore più che raggiungere una colorazione più intensa, presentava sulla superficie delle macchie decolorate. Questo effetto si fonda sul meccanismo di silenziamento dell’RNA, determinato dalla presenza di RNA aberranti a doppio filamento; essi una volta arrivati nel citoplasma degradano una delle due catene.
È proprio questo il principio sul quale si fondano i successivi studi genomici che coinvolgono come mezzo l’RNA. E pensare che non siamo nemmeno arrivati a parlare del gioiellino finale dell’editing genetico!!
La vera rivoluzione in questo campo è arrivata nel 2012 con la scoperta del sistema “Crispr-Cas9”, che ha messo in secondo piano i sistemi di editing “Zinc-finger” e “TALEN” che erano stati utilizzati fino ad allora. Crispr-Cas9 ha dimostrato, fin da subito, una potenzialità e versatilità fino a poco prima inimmaginabili! Si utilizza un RNA guida che riesce a collocare nel punto giusto l’enzima di restrizione Crispr-Cas9, il quale taglia il frammento di DNA da modificare; il taglio viene ricucito dalla cellula mediante un DNA toppa, creato da noi e costituito da geni sani al posto di quelli mutati, trasferito attraverso vettori virali e non virali.
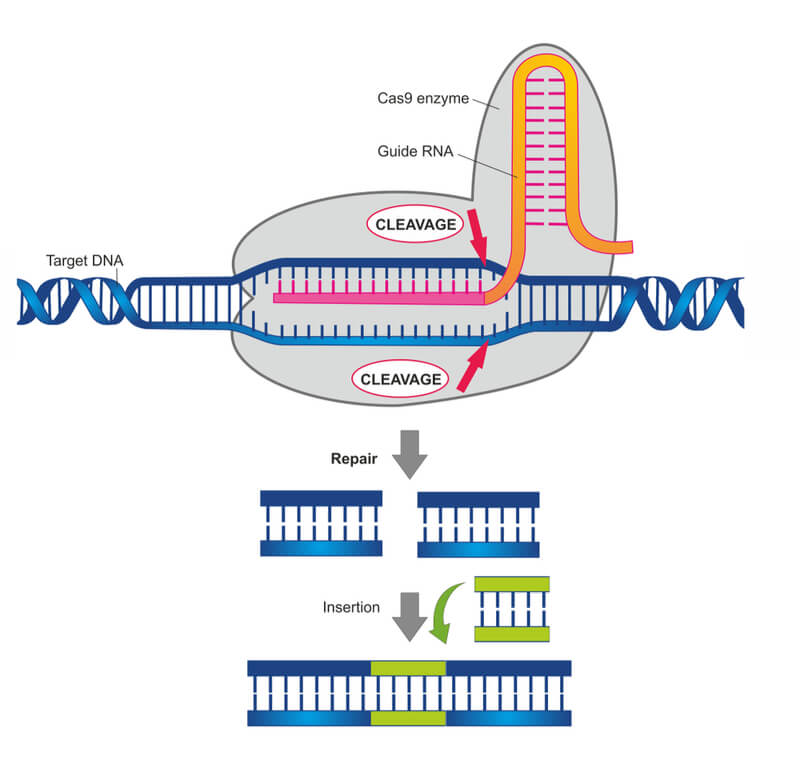
E pensare che grazie a questo sistema qualunque tipo di cellula vegetale, animale, inclusa quella umana, può essere modificata geneticamente e la correzione può avvenire anche per un singolo e minimo errore, e ovunque nel genoma. Inoltre, questa tecnica è facile da utilizzare, veloce ed economica, il che ne amplia le potenzialità in ambito terapeutico.
Ma quali sono stati effettivamente i risultati raggiunti nel mondo della medicina?
Grazie alle geniali scoperte dell’editing genomico i passi in avanti sono stati moltissimi; attualmente sono aperti ben 32 studi differenti di trial clinici che si impegnano nel trovare cure a malattie quali tumori solidi, leucemie e anemia falciforme, tutte caratterizzate da mutazioni del DNA con spesso assenza o mancata attività di meccanismi di riparazione.
La strada da fare è ancora molto lunga, ma tutte queste scoperte di editing genomico fanno crescere in noi la speranza che un domani la medicina possa raggiungere un punto di svolta: garantire cure migliori e più specifiche per ogni tipo di patologia.
Elisabetta Morgante & Raffaele Negri, 4° H